原文信息:
Hao Geng, Ce Matthew Shi,Health policy, price regulation, and innovation: Evidence from China’s vaccine industry. Journal of Development Economics, Volume 167, 2024,
图片来源:
01
引言
尽管发展中国家人口占全球人口的84%,其在全球范围内可预防的死亡人数超过90%,但为中低收入国家开发疫苗一直是一个长期的全球挑战,私人公司往往缺乏进行此类投资的动机。根据世界卫生组织的数据,2005年,私营企业占全球卫生研发支出的59%,其中不到5%用于解决发展中国家特有的卫生问题。一般来说,政府公共卫生政策可以通过市场规模机制来影响创新,但药品价格的昂贵往往导致发展中国家政府进行价格管制,从而限制市场增长并减少私人创新激励。
本文介绍了中国公共疫苗体系的一项重大改革,即2008年至2009年实施的扩大免疫计划,这项计划的特点是引入了疫苗价格管制,即政府为新的计划所覆盖疾病设定每剂疫苗的固定价格,而自费私营部门疫苗的价格不受价格管制。这项政策改革提供了一个独特的准自然实验环境,利用双重差分法以检验政府政策对创新活动的影响。
02
制度背景
2.1. EPI在中国的发展
1978年后,中国政府通过大规模公共疫苗计划EPI为某些疾病提供免费疫苗。1978年的计划里包括四种疫苗:BCG(预防结核病)、口服脊髓灰质炎病毒疫苗(OPV)、白喉-破伤风-百日咳全细胞疫苗(DTwP)和麻疹疫苗,而乙型肝炎疫苗于2002年被列入计划免疫。免疫计划所覆盖的疫苗被称为第一类疫苗,由省级政府集体采购,同时也有自费接种的第二类疫苗,这种疫苗自愿接种,由地方各级卫生部门采购,并且价格不受管制。
本文研究了2008—2009年中国免疫计划(EPI)的一项重大改革。2008年中国政府把甲型肝炎、甲型和丙型脑膜炎球菌病、日本脑炎,以及针对麻疹、腮腺炎和风疹的联合疫苗纳入到免疫计划中。它还扩大到为流行地区的高危人群接种炭疽、钩端螺旋体和肾综合征出血热疫苗。此外,它用无细胞DTP(DTaP)疫苗取代了现有的DTwP疫苗。重要的是,中央政府将MMR和DTP等疾病的疫苗接种率提高到90%以上,并在0至14岁的儿童中普及脑膜炎球菌病、日本脑炎和甲型肝炎的疫苗接种。因此,在保持其他因素不变的情况下,国家计划的扩大可以增加受影响疫苗的市场规模。
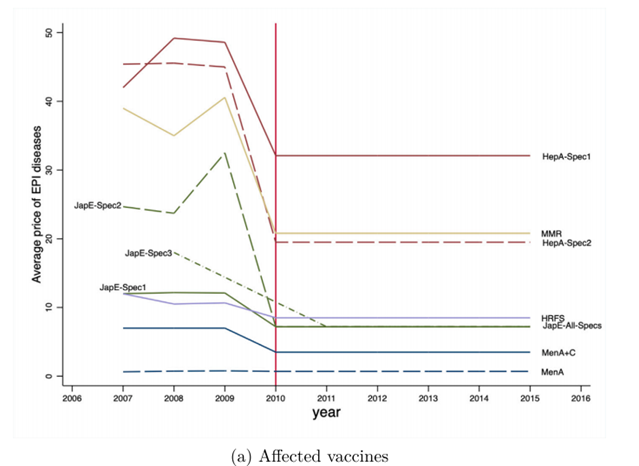
特别是,中央政府根据成本加成定价法(即考虑制造、销售和运营的经济成本加上固定利润率)为每种新的EPI覆盖的疫苗设定了固定价格。这对第一类疫苗的采购价格产生了很大影响,这些疫苗价格平均下降了30%,明显低于美国和欧洲国家的同类疫苗。相比之下,主要由市场力量决定的不受监管的第2类疫苗的价格随着时间的推移呈现平稳上涨趋势。
2.2中国的疫苗产业
截至2015年,在46家注册的疫苗制造商中,国有企业在疫苗创新和生产中发挥着重要作用。中国国药集团旗下位于北京、长春、成都、兰州、上海和武汉的六家国有生物研究所提供了85%—90%的第一类疫苗剂量,而国际疫苗公司向中国提供的很少,因为政府不鼓励外国公司供应EPI覆盖的疫苗。但国内私营企业和外资企业在第二类疫苗市场有很大的影响力,如下图所示,随着时间的推移,国际公司负责供应9.7%的第二类疫苗,并占据了18.6%至40.7%的市场收入。国内私营企业提供了57%的此类疫苗,占市场收入的32.7%至48.8%。
近年来,中国疫苗产业在创新能力方面取得了显著增长。例如,中国企业是开发世界卫生组织批准的乙脑和戊型肝炎等疾病疫苗的先驱。研究表明,中国的疫苗创新能力在发展中国家中排名第二,仅次于印度。
03
数据和实证框架
3.1.1 疫苗临床试验数据
作者使用疫苗临床试验数据来调查研发对中国疫苗政策改革的反应。在基础研究和临床前试验之后,开始新的临床试验标志着药物研发进入到最重要和最昂贵阶段。只有在临床试验取得有利结果后,中国的疫苗生产商才能申请新产品的生产批准。
临床试验数据来自国家药品监督管理局下属的药品审评中心,该中心和省级部门一起负责监管疫苗供应链。作者从该中心网站上搜集数据,共获得1296份新疫苗临床试验记录,利用疫苗的名称来识别其预防的疾病及其为政府提供的第一类疫苗或自费第二类疫苗;利用申请人的姓名来识别所有权类型(国有企业或国内私营企业)。最终识别出36种疾病(包括疾病组合),对于对几种疾病提供保护的组合疫苗,我们为组合中的每种疾病都记录了一次新的疫苗试验。由于2016年中国对疫苗系统进行了改革,影响了第二类疫苗(对照组)的采购,因此没有使用2015之后的数据。
3.1.2 产品层面数据
作者使用详细的产品层面数据来研究疫苗政策如何影响企业收入和疫苗产品的市场规模。通过在国家药品监督管理局下属的中国食品药品检定研究院维护的数据库中获取疫苗批次发布记录,对于每个批次发布记录,收集产品名称、发布日期、制造商名称和生产数量。关于疫苗采购价格,作者通过在财政部下属的中国政府集中采购平台上搜索2007年至2015年的官方采购文件来手工收集数据,获得了66%的疫苗产品的价格信息。对于缺失的价格信息(大多数是第二类疫苗),通过计算其他生产商在同一年生产的疫苗产品的平均价格来估算,或者通过使用滞后的产品价格来估算。
3.2 描述性统计
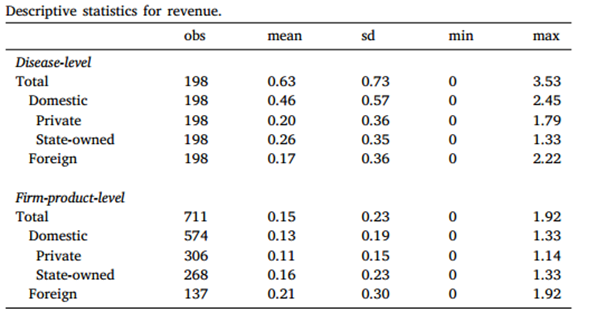
表1列出了新疫苗临床试验数量的汇总统计数据。在2005-2015年期间,有33种疫苗至少进行了一次新的临床试验。平均而言,每种疫苗每年有0.83项新的临床试验,而11.2%的临床试验是受政策影响的六种疫苗。从2005年到2009年,有23.7%的新试验针对这六种疫苗,然而,在2009年之后,只有4.8%与这六种疫苗有关。这表明,免疫计划改革导致新计划所覆盖的疫苗研发大幅减少。
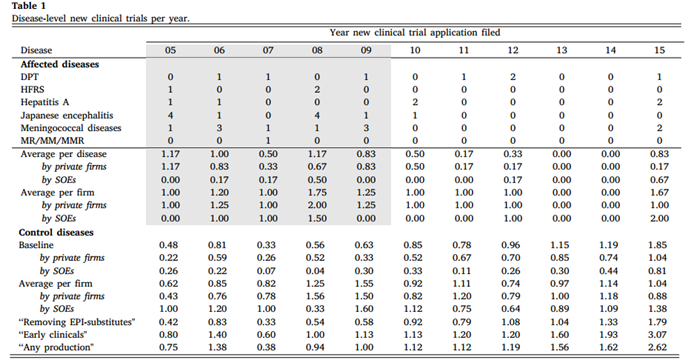
表3列出了总市场层面、企业产品层面和不同类型企业所有权的收入信息汇总统计数据。平均而言,针对特定疾病的疫苗一年的市场总收入为6.4亿元人民币,其中75%由国内公司共同获得,国有企业和国内私营企业会瓜分市场。
3.3 实证策略
本文使用双重差分法将2008-2009年中国免疫计划改革实施前后,受政策影响的新疫苗临床试验数量与未受影响的新试验数量进行了比较。由于主要因变量是计数数据,使用泊松模型进行估计,模型如下:
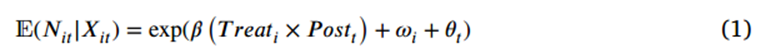

本文主要目标之一是研究市场规模在政策对疫苗研发影响中所起的作用,如果价格监管是减少疫苗研发的主导力量,那么研发减少的程度应该取决于引入价格管制后疫苗采购价格下降的程度。因此,作者又使用了广义DID进行估计,
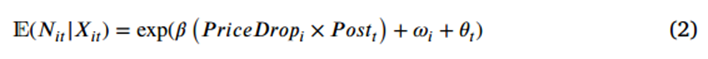
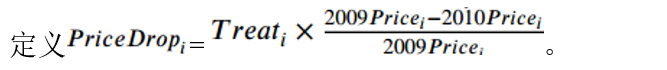
此外,作者直接考察了政策对当前实际收入所代表的市场规模的影响:
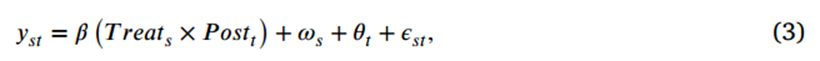
04
实证结果
4.1 基准结果
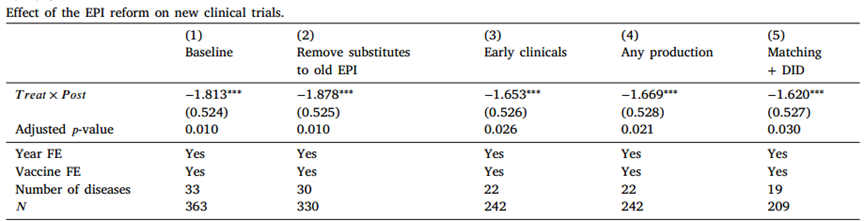
从表中可以看出,系数β为负且高度显著,估计表明,政策实施后,新疫苗临床试验的平均数量急剧下降,下降了83.7%。第2列将可通过第1类和第2类疫苗预防的三种疾病排除在对照组之外。结果(−1.878)与基线估计值相似。在第3列中,重点关注技术更成熟的疫苗,以及改革前至少一项新疫苗临床试验。第4列选择了2007-2015年生产的19种疫苗。第5栏中使用了改革前研发水平和趋势相似的疫苗的匹配样本,并获得了相似的估计值。这些估计表明,免疫计划改革导致受影响疾病的新试验减少了80.8%—81.5%。
4.2 政策对市场收入的影响
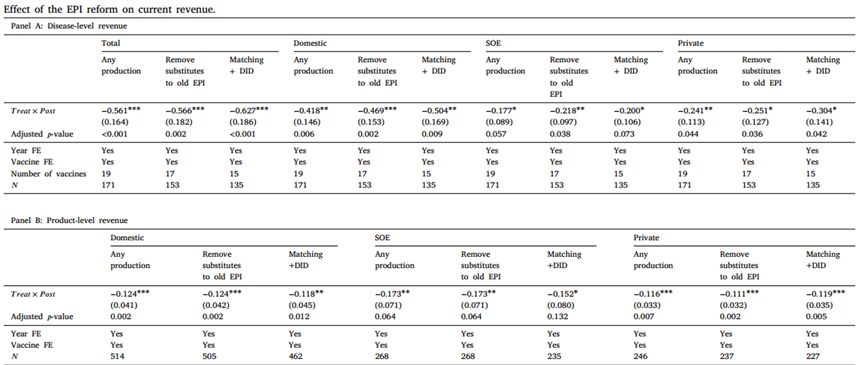
处理组包括针对6种受影响疾病的8种疫苗产品,对照组包括针对未受影响的疾病的11种疫苗,这些疫苗的数据可用于计算收入。由于可用数据有限,我们的观测时间也减少了两年(2005年和2006年)。在第1栏中,估计表明,平均而言,免疫计划改革导致受影响疫苗的年市场收入大幅减少5.61亿元人民币。在第2栏中,从对照组中删除了两种针对可通过第2类疫苗和已有的第1类疫苗预防的联合疫苗,估计值(−0.566)与基线结果相当,具有高度显著性。在第4栏至第6栏中,研究政策对国内企业市场收入的影响,估计表明,受影响疫苗的国内公司总收入平均每年减少超过4亿元人民币。考虑到政策前时期受影响疫苗的平均市场收入为2.76亿元人民币,这些估计意味着改革后,国内公司的收入下降了100%以上。
05
结论
本文为中国这个发展中大国的重大卫生政策改革对疫苗开发的影响提供了新的实证证据。研究结果表明,中国的免疫计划改革使受影响疫苗的新临床试验数量减少了83%。研发工作的大幅减少是由私营公司投资的变化和政府实施的药品价格监管推动的。总的来说,在发展中国家,私营企业确实对政策诱导的市场激励做出了在创新方面的反应。尽管如此,扩大健康计划的市场扩张效应可以通过旨在控制医疗成本的价格管制来抵消。
本文评估了政策引发的创新是否会导致社会福利损失。与Finkelstein(2004)一致,福利分析表明,对于少数疾病,研发投入的减少会提高福利,因为现有技术在疫苗质量方面几乎没有改进的空间。然而,由于对使用不太成熟技术的疫苗进行更多投资可以提高疫苗质量,中国免疫计划改革的长期影响可能对A和C群脑膜炎球菌病等疾病产生负面影响。需要注意的是,本文福利分析没有考虑研发活动可能产生的溢出效应。特别是,在一个领域的私人研发投资(例如开发一种疾病的疫苗)可以帮助企业获得其他相关领域的技术升级和累积创新所需的知识。
推文作者:李俊洁 中国社会科学院大学数量经济学2023级硕士生
Abstract
About 11% of the Chinese population are rural-urban This paper investigates the effect of policy-induced market incentives on pharmaceutical innovation in the context of developing countries, where substantial health challenges persist but research and development (R&D) efforts remain limited. We exploit the quasi-experimental setting of a major reform in China’s public vaccine system, which involved expanding vaccine coverage while imposing price controls on affected products. Using newly collected data on vaccine clinical trials and revenues, we estimate that China’s public vaccine program expansion in 2008–2009 led to an 83% decrease in new vaccine clinical trials for the policy-affected diseases. This decrease can be attributed to the government’s price regulation, which greatly reduced the market revenue of the affected vaccines. Our welfare analysis indicates that for some affected diseases, reducing innovation is welfare-enhancing as the reform has curbed potentially wasteful R&D spending. However, for one disease, the policy-induced reduction in innovation is socially harmful because continued innovation can lead to long-run social benefits by generating more effective products.
声明:推文仅代表文章原作者观点,以及推文作者的评论观点,并不代表香樟经济学术圈公众号平台的观点。
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 